Какие суждения верны витамины являются кофакторами
Запишите пропущенные слова:
1. Структурная функция белков проявляется в том, что (_).
2. Рецепторная функция белков проявляется в том, что (_).
3. Регуляторная функция белков проявляется в том, что (_).
4. Каталитическая функция белков проявляется в том, что (_).
5. Транспортная функция белков проявляется в том, что (_).
6. Двигательная функция белков проявляется в том, что (_).
7. Энергетическая функция белков проявляется в том, что (_).
8. Запасающая функция белков проявляется в том, что (_).
9. Защитная функция белков проявляется в том, что (_).
Задание 8. «Активный центр фермента»
Рассмотрите рисунок и ответьте на вопросы:
- Что обозначено на рисунке под цифрами 1 — 4?
- Как называется участок фермента, взаимодействующий с молекулой субстрата?
- Какая структура у белков-ферментов?
- Почему при изменении температуры и рН изменяется каталитическая активность ферментов?
- Почему ферменты специфичны?
- Чем гипотеза Фишера отличается от гипотезы Кошланда?
Задание 9. «Белки»
Запишите номера тестов, против каждого – правильные варианты ответа
Тест 1. На первом месте по массе из органических веществ в клетке находятся:
1. Углеводы.
2. Белки.
3. Липиды.
4. Нуклеиновые кислоты.
**Тест 2. В состав простых белков входят следующие элементы:
1. Углерод. 5. Фосфор.
2. Водород. 6. Азот.
3. Кислород. 7. Железо.
4. Сера. 8. Хлор.
Тест 3. Количество различных аминокислот, встречающихся в белках:
1. 170.
2. 26.
3. 20.
4. 10.
**Тест 4. Количество незаменимых для человека аминокислот:
1. Таких аминокислот нет.
2. 20.
3. 10.
4. 7.
**Тест 5. Неполноценные белки — белки:
1. В которых отсутствуют некоторые аминокислоты.
2. В которых отсутствуют некоторые незаменимые аминокислоты.
3. В которых отсутствуют некоторые заменимые аминокислоты.
4. Все известные белки являются полноценными.
Тест 6. Придают аминокислотам свойства:
1. Кислые — радикал, щелочные — аминогруппа.
2. Кислые — аминогруппа, щелочные — радикал.
3. Кислые — карбоксильная группа, — щелочные — радикал.
4. Кислые — карбоксильная группа, щелочные — аминогруппа.
Тест 7. Пептидная связь образуется в результате:
1. Реакции гидролиза.
2. Реакции гидратации.
3. Реакции конденсации.
4. Все выше перечисленные реакции могут привести к образованию пептидной связи.
Тест 8. Пептидная связь образуется:
1. Между карбоксильными группами соседних аминокислот.
2. Между аминогруппами соседних аминокислот.
3. Между аминогруппой одной аминокислоты и радикалом другой.
4. Между аминогруппой одной аминокислоты и карбоксильной группой другой.
**Тест 9. Вторичную структуру белков стабилизируют:
1. Ковалентные.
2. Водородные.
3. Ионные.
4. Такие связи отсутствуют.
**Тест 10. Третичную структуру белков стабилизируют:
1. Ковалентные.
2. Водородные.
3. Ионные.
4. Гидрофильно-гидрофобное взаимодействие.
**Тест 11. При окислении 1 г белка образуются:
1. Вода. 5. Мочевина.
2. Углекислый газ. 6. 38,9 кДж энергии.
3. Аммиак.
4. 17, 6 кДж энергии.
Тест 12. В пробирки с пероксидом водорода поместили кусочек вареной колбасы, хлеба, моркови, рубленого яйца. Кислород выделялся в пробирке:
1. С кусочком вареной колбасы.
2. С кусочком хлеба.
3. С кусочком моркови.
4. С кусочком рубленого яйца.
**Тест 13. Верные суждения:
1. Ферменты специфичны, каждый фермент обеспечивает реакции одного типа.
2. Ферменты универсальны и могут катализировать реакции разных типов.
3. Каталитическая активность ферментов не зависит от рН и температуры.
4. Каталитическая активность ферментов напрямую зависит от рН и температуры.
**Тест 14. Верные суждения:
1. Фермент — ключ, субстрат — замок согласно теории Фишера.
2. Фермент — замок, субстрат — ключ согласно теории Фишера.
3. После каталитической реакции фермент и субстрат распадаются, образуя продукты реакции.
4. После каталитической реакции фермент остается неизменным, субстрат распадается, образуя продукты реакции.
Тест 15. Верное суждение:
1. Витамины являются кофакторами многих ферментов.
2. Все белки являются биологическими катализаторами, ферментами.
3. При замерзании происходит необратимая денатурация ферментов.
4. Ренатурация — утрата трехмерной конфигурации белка без изменения первичной структуры.
Задание 10. «Важнейшие пентозы»
Рассмотрите рисунок и ответьте на вопросы:
1. Какие углеводы изображены на рисунке цифрами 1 — 2?
2. В состав каких органических молекул входят данные пентозы?
Задание 11. «Важнейшие гексозы»
Рассмотрите рисунок и ответьте на вопросы:
1. Какие формы глюкозы изображены на рисунке цифрами 1 — 4?
2. Как называется изомеры, входящие в состав целлюлозы? Гликогена? Крахмала?
Источник
Запишите номера тестов, против каждого – правильные варианты ответа
Тест 1. На первом месте по массе из органических веществ в клетке находятся:
1. Углеводы.
2. Белки.
3. Липиды.
4. Нуклеиновые кислоты.
**Тест 2. В состав простых белков входят следующие элементы:
1. Углерод. 5. Фосфор.
2. Водород. 6. Азот.
3. Кислород. 7. Железо.
4. Сера. 8. Хлор.
Тест 3. Количество различных аминокислот, встречающихся в белках:
1. 170.
2. 26.
3. 20.
4. 10.
**Тест 4. Количество незаменимых для человека аминокислот:
1. Таких аминокислот нет.
2. 20.
3. 10.
4. 7.
**Тест 5. Неполноценные белки — белки:
1. В которых отсутствуют некоторые аминокислоты.
2. В которых отсутствуют некоторые незаменимые аминокислоты.
3. В которых отсутствуют некоторые заменимые аминокислоты.
4. Все известные белки являются полноценными.
Тест 6. Придают аминокислотам свойства:
1. Кислые — радикал, щелочные — аминогруппа.
2. Кислые — аминогруппа, щелочные — радикал.
3. Кислые — карбоксильная группа, — щелочные — радикал.
4. Кислые — карбоксильная группа, щелочные — аминогруппа.
Тест 7. Пептидная связь образуется в результате:
1. Реакции гидролиза.
2. Реакции гидратации.
3. Реакции конденсации.
4. Все выше перечисленные реакции могут привести к образованию пептидной связи.
Тест 8. Пептидная связь образуется:
1. Между карбоксильными группами соседних аминокислот.
2. Между аминогруппами соседних аминокислот.
3. Между аминогруппой одной аминокислоты и радикалом другой.
4. Между аминогруппой одной аминокислоты и карбоксильной группой другой.
**Тест 9. Вторичную структуру белков стабилизируют:
1. Ковалентные.
2. Водородные.
3. Ионные.
4. Такие связи отсутствуют.
**Тест 10. Третичную структуру белков стабилизируют:
1. Ковалентные.
2. Водородные.
3. Ионные.
4. Гидрофильно-гидрофобное взаимодействие.
**Тест 11. При окислении 1 г белка образуются:
1. Вода. 5. Мочевина.
2. Углекислый газ. 6. 38,9 кДж энергии.
3. Аммиак.
4. 17, 6 кДж энергии.
Тест 12. В пробирки с пероксидом водорода поместили кусочек вареной колбасы, хлеба, моркови, рубленого яйца. Кислород выделялся в пробирке:
1. С кусочком вареной колбасы.
2. С кусочком хлеба.
3. С кусочком моркови.
4. С кусочком рубленого яйца.
**Тест 13. Верные суждения:
1. Ферменты специфичны, каждый фермент обеспечивает реакции одного типа.
2. Ферменты универсальны и могут катализировать реакции разных типов.
3. Каталитическая активность ферментов не зависит от рН и температуры.
4. Каталитическая активность ферментов напрямую зависит от рН и температуры.
**Тест 14. Верные суждения:
1. Фермент — ключ, субстрат — замок согласно теории Фишера.
2. Фермент — замок, субстрат — ключ согласно теории Фишера.
3. После каталитической реакции фермент и субстрат распадаются, образуя продукты реакции.
4. После каталитической реакции фермент остается неизменным, субстрат распадается, образуя продукты реакции.
Тест 15. Верное суждение:
1. Витамины являются кофакторами многих ферментов.
2. Все белки являются биологическими катализаторами, ферментами.
3. При замерзании происходит необратимая денатурация ферментов.
4. Ренатурация — утрата трехмерной конфигурации белка без изменения первичной структуры.
Источник
Николай К. · 3 октября 2018
2,4 K
Мои интересы: разнообразны, но можно выделить следующие: литература, история…
Ферменты (биологические катализаторы) — это белки, в молекуле которых имеется активный центр. В этом центре происходит процесс катализа. Активный центр многих ферментов содержит витамин или получаемое из него вещество. То есть витамин — часть фермента и без витаминов ферменты не работают. По своему биологическому действию витамины близки к ферментам, но ферменты образуются клетками организма, а витамины обычно поступают с пищей.
Можно ли принимать пищеварительные ферменты животного происхождения на постоянной основе? Слышал, что из-за них собственные ферменты перестают вырабатываться?
Преподаватель биологических дисциплин, физиолог
Можно, но не нужно. Я бы вообще на вашем месте, их принимал только тогда, когда врач на этом явно настаивает, никакого самолечения. Далеко не самые безобидный и необходимый класс препаратов. А уж тем более для хронического применения. Безусловно есть риск нарушить процесс выработки собственных ферментов. Но дело в том, что их нельзя принимать бездумно, руководствуясь логикой того, что у вас может просто не всегда хорошо переваривается пища. Нужны результаты конкретных анализов, чтобы точно определить, какие ферменты в какой концентрации и когда вам следует принимать, иначе можно сделать только хуже.
Я могу предложить более простой, мягкий, но не менее эффективный, в обычных случаях, способ, основанный на изменении вашего рациона. Ферменты вашей поджелудочной или желчного пузыря не единственные, что участвуют в пищеварении, все же прекрасно знают о кишечной микрофлоре. Поэтому употребляйте кисломолочные продукты, правда, настоятельно рекомендую брать их у частников, а не в магазине. Обычная молочка весьма паршивого качества, дешевле 100 рублей вообще можно даже ничего не брать, у меня от неё, скорее наоборот, тяжесть в животе. К тому же, можно купить в аптеке живую культуру лактобактерий и пить её, в разумных количествах, без фанатизма. Это будет даже правильнее.
Употребляйте побольше продуктов, что стимулируют пищеварение (листовые овощи, особенно, можно овощные соки) и избегайте того, что требует длительного процесса переваривания, вроде красного мяса (кушайте белое), жирного, острого, выраженно сладкого, кислого, солёного. Для конкретных заболеваний ЖКТ есть конкретные диеты, вроде слизевых супов и т.п. Такое тоже лучше обсуждать с врачом.
Откуда в человеческом организме берется АМФ для синтеза АДФ для синтеза АТФ?
АМФ в организме образуется из (парадоксально, но это так!, метаболизм идёт просто по выгодному на данный момент пути) АТФ и аденозина. На аденозин переносится один фосфорный остаток, в результате имеем АМФ (аденозин плюс 1 остаток фосфорной кислоты) и АДФ (аденозинтрифосфат минус 1 остаток фосфорной кислоты).
Однако основной путь синтеза АМФ в организме — de novo, то есть из более простых органических веществ и неорганических молекул. Так, АМФ производится поэтапно разными ферментами из аминокислот аспартата и глицина (поступают в организм с белковой пищей либо синтезируются в организме), глутамина (преобразуется из глицина), двух молекул тетрагидрофолата (с приёмом фолиевой кислоты с пищей), модифицированных разными углеводородными группами, и молекулы углекислого газа, получаемой из воздуха. Постепенно на аминокислотном остове синтезируется молекула ИМФ (инозитол-монофосфат), а из него АМФ. Только АМФ потом идёт на синтез ДНК и РНК, а АТФ синтезируется из АДФ. А АДФ синтезируется из АТФ. Вот так вот.
Существует ли предел совершенства у живого организма, с точки зрения математики и передаваемой из поколения в поколение генетической информации?
Медицинский психолог, психотерапевт, преподаватель биологии, ученый https://vk.c…
У вопрошающего, к сожалению, распространенная ошибка понимания эволюции. Эволюция не имеет цели. Все что она делает, это из того, что есть отбирает то, что имеет максимальную жизнеспособность здесь и сейчас. Эволюция не создает совершенные организмы, эволюция всего лишь повышает уровень приспособленности вида к конкретным условиям в рамках определенных исторических, биологических и химических ограничений. Эволюция не может закончится никогда
Прочитать ещё 1 ответ
Действительно ли помогают химически выведенные витамины ( те, что в аптеке продаются)?
Клинический ординатор-невролог
Суть дела в том, что по химической формуле витамины, синтезированные в лаборатории, не отличаются от тех, которые синтезирует живое растение. Вопрос об их усвоении так же уже давно изучен и в научном сообществе не ставится под сомнение, химически синтезированные аналоги давно применяются для лечения гипо и авитаминозов, и вполне себе эффективны. Но если Вы не доверяете подобным утверждениям и Вам нужны ссылки на исследования, то вот пример : людям давали употреблять киви/апельсины и эквивалентную дозу синтезированного витамина С, затем сравнивали концентрацию витамина С в крови, сперме и мышечной ткани (Carr C. et al. A randomized steady-state bioavailability study of synthetic versus natural(kiwifruct-derived) vitamin C // Nutrients 2013, 5(9), 3684-3695)
Но есть отдельные исключения, например витамин Е. Он действительно усваивается лучше из естественных источников, а все из-за того, что органическая молекула этого витамина имеет несколько стереоизомеров, а точнее 8, в пробирке при синтезе получаются все 8, соответственно усваиваться такой продукт будет хуже, потому что нам нужен всего 1 стереоизомер из 8, а растения синтезируют именно его, обходя стороной остальные.
В качестве исключения со стороны таблетированной формы выступает фолиевая кислота или витамин В9. В естественных источниках содержатся в большинстве своем производные фолатов, полиглутаматы, для их усвоения необходимо их сначала расщепить на составляющие, и делает это специальный фермент глутаматкарбоксипептидаза-2, но он чувствителен к уровню pH и поэтому у отдельных людей его может не хватать, из-за чего собственно и будет страдать усвоение витамина В9. При создании таблеток учитывается этот факт, и используется наиболее легкоусвояемая форма.
Но как уже неоднократно говорилось в подобных вопросах о витаминах, самый важный вопрос заключается в том, нужно ли Вам принимать витамины дополнительно или нет, и здесь все зависит от многих факторов, но по большей части от Вашего рациона. И если Вы питаетесь полноценно и сбалансировано(а здесь уже встает вопрос о том, что же такое сбалансированное и полноценное питание), то единственное о чем Вам стоит беспокоится, проживая в северных широтах, это возможный дефицит витамина D, ввиду отсутствия достаточного количества ультрафиолета в зимне-осеннее время.
Источник

Химический состав клетки Семинар

1. Какие элементы называются биогенными? Сколько их? 2. На какие группы делятся макроэлементы? 3. Чем ковалентные связи отличаются от водородных? 4. Почему лед образуется на поверхности воды? 5. Какие вещества называются гидрофобными? Гидрофильными? 6. Какой заряд на атоме кислорода и на атомах водорода в молекуле воды? Почему? 7. Сколько водородных связей может образовывать одна молекула воды? 8. Почему ион натрия имеет положительный заряд? 9. Почему ион хлора имеет отрицательный заряд?
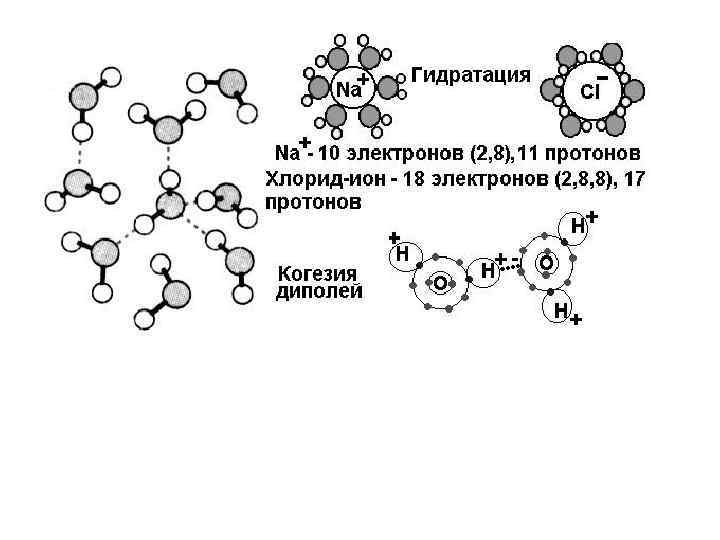

1. К моносахаридам относятся: 1. Крахмал. 5. Свекловичный сахар (сахароза). 2. Гликоген. 6. Мальтоза. 3. Глюкоза. 7. Молочный сахар (лактоза). 4. Дезоксирибоза. 8. Рибоза. 2. К полисахаридам относятся: 1. Крахмал. 5. Рибоза. 2. Гликоген. 6. Мальтоза. 3. Глюкоза. 7. Молочный сахар (лактоза). 4. Дезоксирибоза. 8. Целлюлоза. 3. К дисахаридам относятся: 1. Крахмал. 2. Свекловичный сахар (сахароза). 3. Глюкоза. 4. Дезоксирибоза. 5. Хитин. 6. Мальтоза. 7. Молочный сахар (лактоза). 8. Целлюлоза.

Какие вещества являются моносахаридами, полисахаридами, дисахаридами? 1 2 3
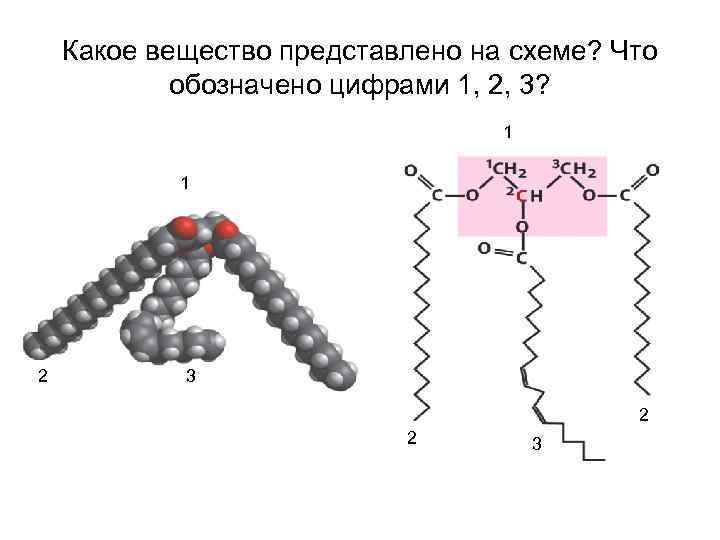
Какое вещество представлено на схеме? Что обозначено цифрами 1, 2, 3? 1 1 2 3 2 2 3

1. При полном сгорании 1 г. вещества выделилось 38, 9 к. Дж энергии. Это вещество относится: 1. К углеводам. 2. К жирам. 3. Или к углеводам, или к липидам. 4. К белкам. 2. Основу клеточных мембран образуют: 1. Жиры. 2. Фосфолипиды. 3. Воска. 4. Липиды. 3. Утверждение: «Фосфолипиды — сложные эфиры глицерина (глицерола) и жирных кислот»: Верно. Ошибочно.

4. Липиды выполняют в организме следующие функции: 1. Структурную. 5. Некоторые являются ферментами. 2. Энергетическую. 6. Источник метаболической воды 3. Теплоизолирующую. 7. Запасающую. 4. Некоторые — гормоны. 8. К ним относятся витамины A, D, E, K. 5. Молекула жира состоит из остатков: 1. Аминокислот. 2. Нуклеотидов. 3. Глицерина. 4. Жирных кислот. 6. Гликопротеины — это комплекс: 1. Белков и углеводов. 2. Нуклеотидов и белков. 3. Глицерина и жирных кислот. 4. Углеводов и липидов.
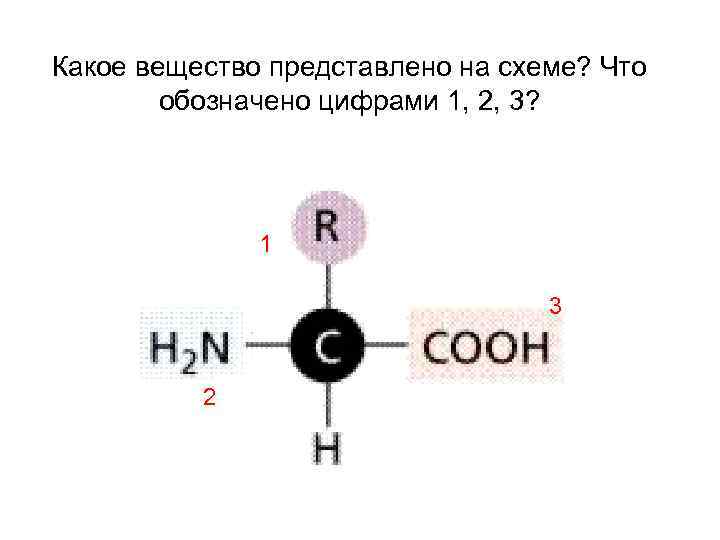
Какое вещество представлено на схеме? Что обозначено цифрами 1, 2, 3? 1 3 2
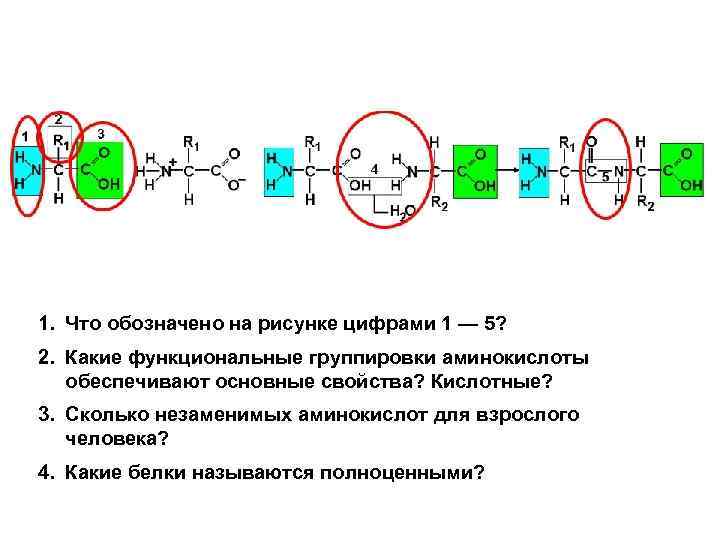
1. Что обозначено на рисунке цифрами 1 — 5? 2. Какие функциональные группировки аминокислоты обеспечивают основные свойства? Кислотные? 3. Сколько незаменимых аминокислот для взрослого человека? 4. Какие белки называются полноценными?

1. На первом месте по массе из органических веществ в клетке находятся: 1. Углеводы. 2. Белки. 3. Липиды. 4. Нуклеиновые кислоты. 2. В состав простых белков входят следующие элементы: 1. Углерод. 5. Фосфор. 2. Водород. 6. Азот. 3. Кислород. 7. Железо. 4. Сера. 8. Хлор. 3. Количество различных стандартных аминокислот, встречающихся в белках: 1. 170. 2. 26. 3. 20. 4. 10.

4. Количество незаменимых для человека аминокислот: 1. Таких аминокислот нет. 2. 20. 3. 10. 4. 7. 5. Неполноценные белки — белки: 1. В которых отсутствуют некоторые аминокислоты. 2. В которых отсутствуют некоторые незаменимые аминокислоты. 3. В которых отсутствуют некоторые заменимые аминокислоты. 4. Все известные белки являются полноценными. 6. Придают аминокислотам свойства: 1. Кислые — радикал, щелочные — аминогруппа. 2. Кислые — аминогруппа, щелочные — радикал. 3. Кислые — карбоксильная группа, — щелочные — радикал. 4. Кислые — карбоксильная группа, щелочные — аминогруппа.

7. Пептидная связь образуется в результате: 1. Реакции гидролиза. 2. Реакции гидратации. 3. Реакции конденсации. 4. Все выше перечисленные реакции могут привести к образованию пептидной связи. 8. Пептидная связь образуется: 1. Между карбоксильными группами соседних аминокислот. 2. Между аминогруппами соседних аминокислот. 3. Между аминогруппой одной аминокислоты и радикалом другой. 4. Между аминогруппой одной аминокислоты и карбоксильной группой другой. 9. Вторичную структуру белков стабилизируют: 1. Ковалентные. 2. Водородные. 3. Ионные. 4. Такие связи отсутствуют.

10. Третичную структуру белков стабилизируют: 1. Ковалентные. 2. Водородные. 3. Ионные. 4. Гидрофильно-гидрофобное взаимодействие. 5. Все выше перечисленные виды связей. 11. Верные суждения: 1. Ферменты специфичны, каждый фермент обеспечивает реакции одного типа. 2. Ферменты универсальны и могут катализировать реакции разных типов. 3. Каталитическая активность ферментов не зависит от р. Н и температуры. 4. Каталитическая активность ферментов напрямую зависит от р. Н и температуры. 12. Верное суждение: 1. Все белки являются биологическими катализаторами, ферментами. 2. Ренатурация — утрата трехмерной конфигурации белка без изменения первичной структуры. 3. Витамины являются коферментами многих ферментов.

Какое вещество представлено на рисунке? Что обозначено цифрами 1, 2, 3, 4? 3 4 2 1
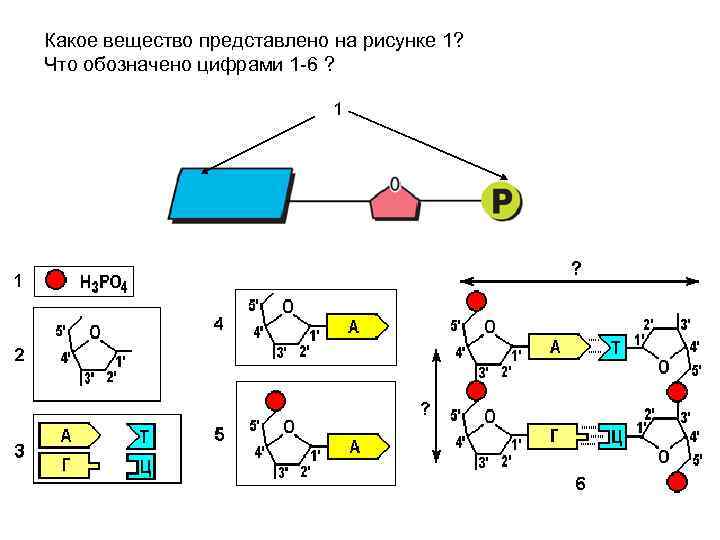
Какое вещество представлено на рисунке 1? Что обозначено цифрами 1 -6 ? 1

1. ДНК в клетках эукариот содержится: 1. В цитоплазме. 5. В пластидах. 2. В ядре. 6. В комплексе Гольджи. 3. В рибосомах. 4. В митохондриях. 2. Размеры молекулы ДНК у человека: 1. Ширина 20 мкм, длина до 8 см. 2. Ширина 2 мкм, длина до 8 см. 3. Ширина 20 нм, длина до 8 см. 4. Ширина 2 нм, длина до 8 см. 3. В состав молекулы ДНК входят пуриновые основания: 1. Аденин. 2. Гуанин. 3. Тимин. 4. Цитозин.

4. Фрагмент ДНК содержит 30000 нуклеотидов. Для удвоения фрагмента потребуется свободных нуклеотидов: 1. 60000. 2. 45000. 3. 30000. 4. 15000. 5. Нуклеотиды ДНК соединены в одну цепь: 1. Через остаток фосфорной кислоты одного нуклеотида и 3′ атом дезоксирибозы другого. 2. Через остаток фосфорной кислоты одного нуклеотида и азотистое основание другого. 3. Через остатки фосфорной кислоты соседних нуклеотидов. 4. Через дезоксирибозы соседних нуклеотидов.

6. Фрагмент ДНК содержит 30000 А-нуклеотидов. Для удвоения фрагмента потребуется: 1. А — 60000, Т — 60000. 2. А — 30000, Т — 30000. 3. А — 15000, Т — 15000. 4. Данных для ответа недостаточно. 7. Фрагмент ДНК содержит 30000 А-нуклеотидов и 40000 Цнуклеотидов. В данном фрагменте Т- и Г-нуклеотидов: 1. Т — 40000, Г — 30000. 2. Т — 30000, Г — 40000. 3. Т — 60000, Г — 80000. 4. Данных для ответа недостаточно. 8. Предложили модель строения молекулы ДНК в 1953 году: 1. Ф. Крик. 2. Г. Мендель. 3. Т. Морган. 4. Д. Уотсон.

9. Функции ДНК в клетке: 1. Один из основных источников энергии. 2. Принимает непосредственное участие в синтезе белков. 3. Обеспечивает синтез углеводов и липидов в клетке. 4. Участвует в хранении и передаче наследственной информации. 10. Верные суждения: 1. Цепи нуклеотидов в молекуле ДНК антипараллельны. 2. Между А- и Т-нуклеотидами 2 водородные связи, между Г- и Цнуклеотидами 3 водородные связи. 3. А- и Т-нуклеотиды относятся к пиримидиновым нуклеотидам. 4. В состав нуклеотидов ДНК входит сахар рибоза.
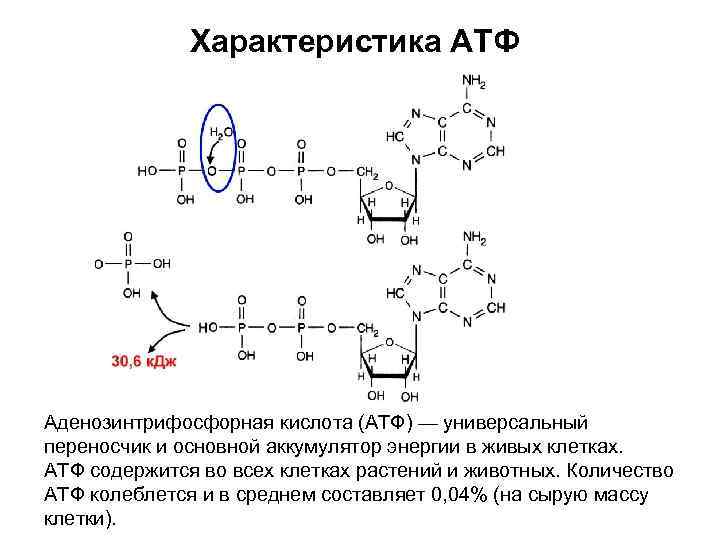
Характеристика АТФ Аденозинтрифосфорная кислота (АТФ) — универсальный переносчик и основной аккумулятор энергии в живых клетках. АТФ содержится во всех клетках растений и животных. Количество АТФ колеблется и в среднем составляет 0, 04% (на сырую массу клетки).
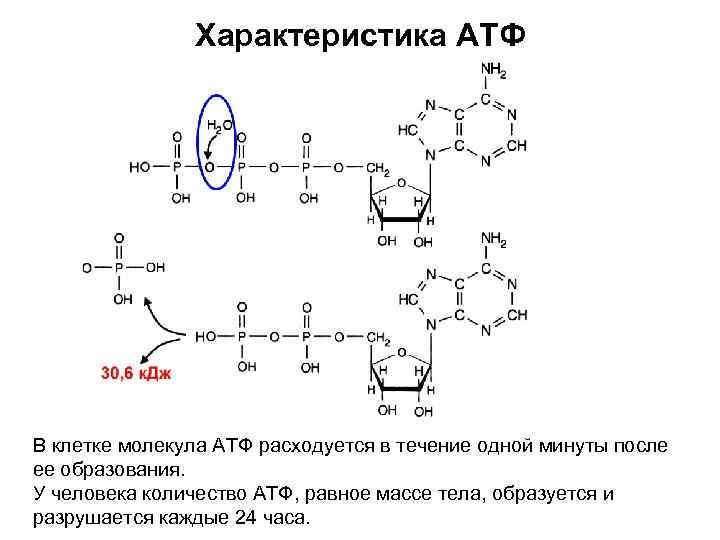
Характеристика АТФ В клетке молекула АТФ расходуется в течение одной минуты после ее образования. У человека количество АТФ, равное массе тела, образуется и разрушается каждые 24 часа.
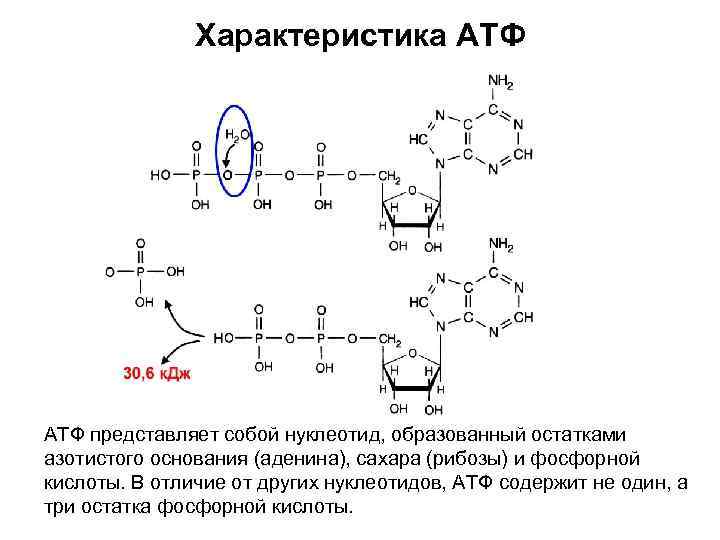
Характеристика АТФ представляет собой нуклеотид, образованный остатками азотистого основания (аденина), сахара (рибозы) и фосфорной кислоты. В отличие от других нуклеотидов, АТФ содержит не один, а три остатка фосфорной кислоты.
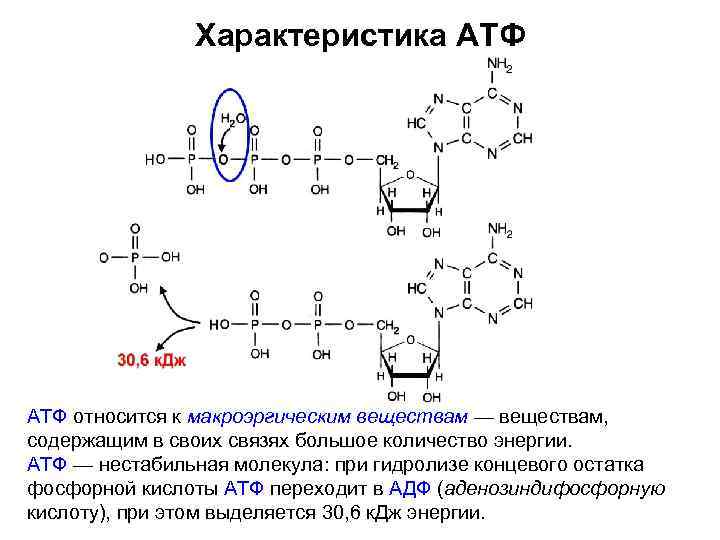
Характеристика АТФ относится к макроэргическим веществам — веществам, содержащим в своих связях большое количество энергии. АТФ — нестабильная молекула: при гидролизе концевого остатка фосфорной кислоты АТФ переходит в АДФ (аденозиндифосфорную кислоту), при этом выделяется 30, 6 к. Дж энергии.
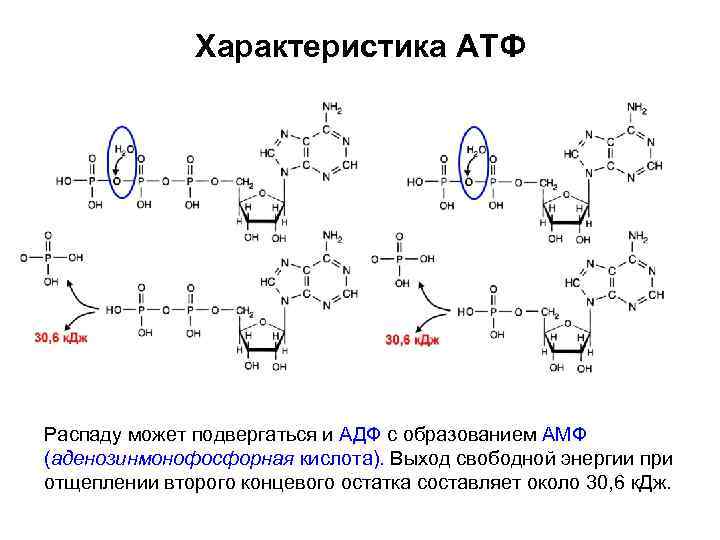
Характеристика АТФ Распаду может подвергаться и АДФ с образованием АМФ (аденозинмонофосфорная кислота). Выход свободной энергии при отщеплении второго концевого остатка составляет около 30, 6 к. Дж.
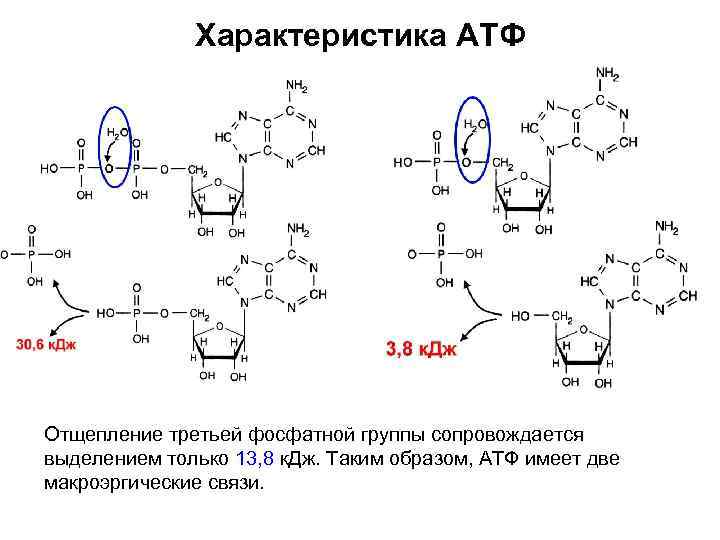
Характеристика АТФ Отщепление третьей фосфатной группы сопровождается выделением только 13, 8 к. Дж. Таким образом, АТФ имеет две макроэргические связи.

Какие суждения верны: • Молекула РНК представляет собой неразветвленную полинуклеотидную цепь. • В состав нуклеотидов РНК входит сахар рибоза. • Азотистые основания в РНК представлены аденином, гуанином, тимином и цитозином. • Самые крупные молекулы РНК содержатся в рибосомах, р. РНК. • Нуклеотиды РНК способны образовывать водородные связи между собой, но это внутрицепочечные, а не межцепочечные соединения комплементарных нуклеотидов. • Цепи РНК значительно длиннее молекул ДНК. • РНК обеспечивают синтез белков в клетке.

Какие суждения верны: 8. Молекула РНК состоит из двух комплементарно связанных и антипараллельно направленных полинуклеотидных цепей. 9. Молекулы РНК образуются в результате самоудвоения, репликации. 10. АТФ представляет собой нуклеотид, образованный остатками азотистого основания (аденина), сахара (дезоксирибозы) и фосфорной кислоты. 11. При гидролизе макроэргических связей двух моль АТФ до АМФ выделяется около 160 к. Дж энергии.
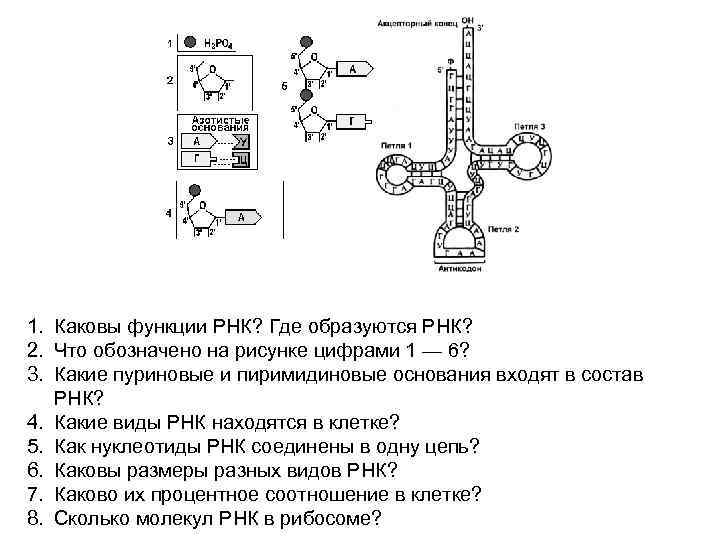
1. Каковы функции РНК? Где образуются РНК? 2. Что обозначено на рисунке цифрами 1 — 6? 3. Какие пуриновые и пиримидиновые основания входят в состав РНК? 4. Какие виды РНК находятся в клетке? 5. Как нуклеотиды РНК соединены в одну цепь? 6. Каковы размеры разных видов РНК? 7. Каково их процентное соотношение в клетке? 8. Сколько молекул РНК в рибосоме?
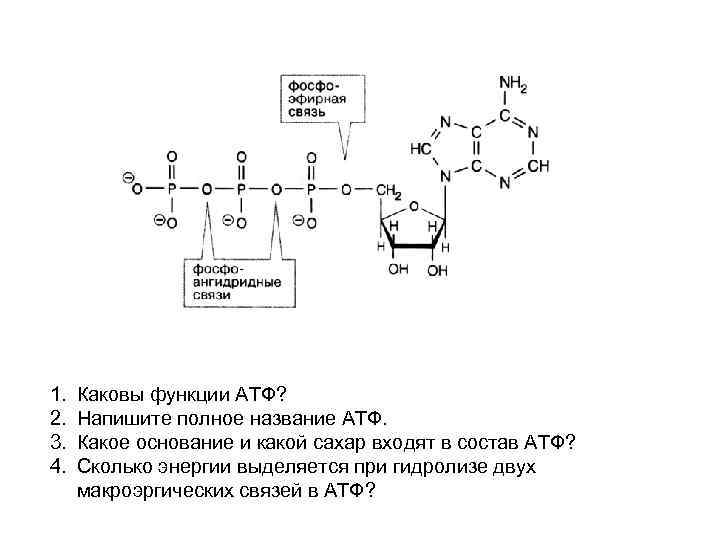
1. 2. 3. 4. Каковы функции АТФ? Напишите полное название АТФ. Какое основание и какой сахар входят в состав АТФ? Сколько энергии выделяется при гидролизе двух макроэргических связей в АТФ?
Источник
