Какой витамин входит в состав фмн и фад
Коферменты в каталитических реакциях осуществляют транспорт различных групп атомов, электронов или протонов. Коферменты связываются с ферментами:
— ковалентными связями;
— ионными связями;
— гидрофобными взаимодействиями и т.д.
Один кофермент может быть коферментом для нескольких ферментов. Многие коферменты являются полифункциональными (например, НАД, ПФ). В зависимости от апофермента зависит специфичность холофермента.
Все коферменты делят на две большие группы: витаминные и невитаминные.
Коферменты витаминной природы– производные витаминов или химические модификации витаминов.
1 группа: тиаминовые – производные витамина В1. Сюда относят:
— тиаминмонофосфат (ТМФ);
— тиаминдифосфат (ТДФ) или тиаминпирофосфат (ТПФ) или кокарбоксилаза;
— тиаминтрифосфат (ТТФ).
ТПФ имеет наибольшее биологическое значение. Входит в состав декарбоксилазы кетокислот: ПВК, a-кетоглутаровая кислота. Этот фермент катализирует отщепление СО2.
Кокарбоксилаза участвует в транскетолазной реакции из пентозофосфатного цикла.
2 группа: флавиновые коферменты, производные витамина В2. Сюда относят:
— флавинмононуклеотид (ФМН);
— флавинадениндинуклеотид (ФАД).
Ребитол и изоалоксазин образуют витамин В2. Витамин В2 и остаток фосфорной к-ты образуют ФМН. ФМН в соединении с АМФ образуют ФАД.
[рис. изоалоксазиновое кольцо соединено с ребитолом, ребитол с фосфорной к-той, а фосфорная к-та – с АМФ]
ФАД и ФМН являются коферментами дегидрогеназ. Эти ферменты катализируют отщепление от субстрата водорода, т.е. участвуют в реакциях окисления–восстановления. Например СДГ – сукцинатдегидрогеназа – катализирует превращение янтарной к-ты в фумаровую. Это ФАД-зависимый фермент. [рис. COOH-CH2-CH2-COOH® (над стрелкой – СДГ, под – ФАД и ФАДН2) COOH-CH=CH-COOH]. Флавиновые ферменты (флавинзависимые ДГ) содержат ФАД, который в них является первоисточником протонов и электронов. В процессе хим. реакций ФАД превращается в ФАДН2. Рабочей частью ФАД является 2 кольцо изоалоксазина; в процессе хим. реакции идет присоединение двух атомов водорода к азотам и перегруппировка двойных связей в кольцах.
3 группа: пантотеновые коферменты, производные витамина В3 – пантотеновой кислоты. Входят в состав кофермента А, НS-КоА. Этот кофермент А является коферментом ацилтрансфераз, вместе с которой переносит различные группировки с одной молекулы на другую.
4 группа: никотинамидные, производные витамина РР — никотинамида:
Представители:
— никотинамидадениндинуклеотид (НАД);
— никотинамидадениндинуклеотидфосфат (НАДФ).
Коферменты НАД и НАДФ являются коферментами дегидрогеназ (НАДФ-зависимых ферментов), например малатДГ, изоцитратДГ, лактатДГ. Участвуют в процессах дегидрирования и в окислительно-восстановительных реакциях. При этом НАД присоединяет два протона и два электрона, и образуется НАДН2.
Рис. рабочей группы НАД и НАДФ: рисунок витамина РР, к которому присоединяется один атом Н и в результате происходит перегруппировка двойных связей. Рисуется новая конфигурация витамина РР + Н+]
5 группа: пиридоксиновые, производные витамина В6. [рис. пиридоксаля. Пиридоксаль+ фосфорная к-та= пиридоксальфосфат]
— пиридоксин;
— пиридоксаль;
— пиридоксамин.
Эти формы взаимопревращаются в процессе реакций. При взаимодействии пиридоксаля с фосфорной кислотой получается пиридоксальфосфат (ПФ).
ПФ является коферментом аминотрансфераз, осуществляет перенос аминогруппы от АК на кетокислоту – реакция переаминирования. Также производные витамина В6 входят как коферменты в состав декарбоксилаз АК.
Коферменты невитаминной природы – вещества, которые образуются в процессе метаболизма.
1) Нуклеотиды – УТФ, УДФ, ТТФ и т.д. УДФ-глюкоза вступает в синтез гликогена. УДФ-гиалуроновая к-та используется для обезвреживания различных веществ в трансверных реакциях (глюкоуронил трансфераза).
2) Производные порфирина (гем): каталаза, пероксидаза, цитохромы и т.д.
3) Пептиды. Глутатион – это трипептид (ГЛУ-ЦИС-ГЛИ), он участвует в о-в реакциях, является коферментом оксидоредуктаз (глутатионпероксидаза, глутатионредуктаза). 2GSH«(над стрелкой 2Н) G-S-S-G. GSH является восстановленной формой глутатиона, а G-S-S-G – окисленной.
4) Ионы металлов, например Zn2+ входит в состав фермента АлДГ (алкогольдегидрогеназы), Cu2+ — амилазы, Mg2+ — АТФ-азы (например, миозиновой АТФ-азы).
Могут участвовать в:
-присоединении субстратного комплекса фермента;
-в катализе;
-стабилизация оптимальной конформации активного центра фермента;
-стабилизация четвертичной структуры.
Источник
Витамин В2
(рибофлавин) впервые был выделен из молока и ряда других пищевых продуктов. В
зависимости от источника получения витамин В2 называли по-разному,
хотя по существу это было одно и то же соединение: лактофлавин (из молока),
гепатофлавин (из печени), овофлавин (из белка яиц), вердофлавин (из растений).
Химический синтез витамина В2 был осуществлен в 1935 г. Р. Куном.
Растворы витамина В2 имеют оранжево-желтую окраску и характеризуются
желто-зеленой флюоресценцией.
В основе
молекулы рибофлавина лежит гетероциклическое соединение изоаллоксазин
(сочетание бензольного, пиразинового и пиримидинового колец), к которому в
положении 9 присоединен пятиатомный спирт рибитол. Химическое название
«рибофлавин» отражает наличие рибитола и желтой окраски препарата ,
рациональное название его 6,7-диметил-9-D-рибитилизоаллоксазин.
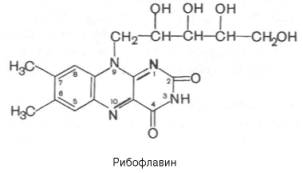
Рибофлавин
хорошо растворим в воде, устойчив в кислых растворах, но легко разрушается в
нейтральных и щелочных растворах. Он весьма чувствителен к видимому и
УФ-излучению и сравнительно легко подвергается обратимому восстановлению,
присоединяя водород по месту двойных связей и превращаясь в бесцветную
лейкоформу. Это свойство рибофлавина легко окисляться и восстанавливаться лежит
в основе его биологического действия в клеточном метаболизме.
Клинические
проявления недостаточности рибофлавина лучше всего изучены на экспериментальных
животных. Помимо остановки роста, выпадения волос (алопеция), характерных для
большинства авитаминозов, специфичными для авитаминоза В2 являются
воспалительные процессы слизистой оболочки языка (глоссит), губ, особенно у
углов рта, эпителия кожи и др. Наиболее характерны кератиты, воспалительные
процессы и усиленная васкуляризация роговой оболочки, катаракта (помутнение
хрусталика). При авитаминозе В2 у людей развиваются общая мышечная
слабость и слабость сердечной мышцы.
Согласно данным К. Яги, существует прямая связь между степенью недостаточности
рибофлавина у животных и накоплением в крови продуктов перекисного окисления
липидов (ПОЛ), развитием атеросклероза и катаракты. Эти нарушения, по мнению
автора, указывают на важную роль флавопротеинов в молекулярных механизмах
синтеза и распада продуктов ПОЛ.
Биологическая роль. Рибофлавин входит в состав флавиновых коферментов, в
частности ФМН и ФАД , являющихся в свою очередь просте-тическими группами
ферментов ряда других сложных белков – флаво-протеинов. Некоторые флавопротеины
в дополнение к ФМН или ФАД содержат еще прочно связанные неорганические ионы, в
частности железо или молибден, наделенные способностью катализировать транспорт
электронов. Различают 2 типа химических реакций, катализируемых этими
ферментами. К первому относятся реакции, в которых фермент осуществляет прямое
окисление с участием кислорода, т.е. дегидрирование (отщепление электронов и
протонов) исходного субстрата или промежуточного метаболита. К ферментам этой
группы относятся оксидазы L- и D-аминокислот, глициноксидаза, альдегидоксидаза,
ксантиноксидаза и др. Вторая группа реакций, катализируемых флавопротеинами,
характеризуется переносом электронов и протонов не от исходного субстрата, а от
восстановленных пиридиновых коферментов. Ферменты этой группы играют главную
роль в биологическом окислении. В каталитическом цикле изоаллоксазиновый
остаток ФАД или ФМН подвергается обратимому восстановлению с присоединением
электронов и атомов водорода к N1 и N10.
ФМН и ФАД прочно связываются с белковым компонентом, иногда даже
ковалентно, как, например, в молекуле сукцинатдегидрогеназы.
ФМН
синтезируется в организме животных из свободного рибофлавина и АТФ при участии
специфического фермента рибофлавинкиназы:
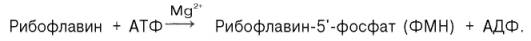
Образование
ФАД в тканях также протекает при участии специфического АТФ-зависимого фермента
ФМН-аденилилтрансферазы. Исходным веществом для синтеза является ФМН:
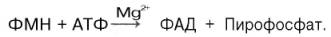
Распространение в природе и суточная потребность. Рибофлавин достаточно широко
распространен в природе. Он содержится почти во всех животных тканях и
растениях; сравнительно высокие концентрации его обнаружены в дрожжах. Из
пищевых продуктов рибофлавином богаты хлеб (из муки грубого помола), семена
злаков, яйца, молоко, мясо, свежие овощи и др.; в молоке он содержится в
свободном состоянии, а в печени и почках животных прочно связан с белками в
составе ФАД и ФМН. Из организма человека и животных рибофлавин выделяется с
мочой в свободном виде. Суточная потребность взрослого человека в рибофлавине
составляет 1,7 мг, в пожилом возрасте и при тяжелой физической работе эта
потребность возрастает.

Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 9 января 2017;
проверки требуют 28 правок.
| Рибофлавин | |
|---|---|
| Систематическое наименование | Рибофлавин; лактофлавин; витамин B2; E101 |
| Хим. формула | C17H20N4O6 |
| Молярная масса | 376,37 г/моль |
| Температура | |
| • плавления | 282 °C |
| Растворимость | |
| • в воде | 0,11 мг/мл при 27,5 °C |
| • в ацетоне | нерастворимы |
| • в диэтиловом эфире | нерастворимы |
| • в хлороформе | нерастворимы |
| • в бензоле | нерастворимы |
| Рег. номер CAS | 83-88-5 |
| PubChem | 493570 |
| Рег. номер EINECS | 201-507-1 |
| SMILES | CC1=CC2=C(C=C1C)N(C3=NC(=O)NC(=O)C3=N2)CC(C(C(CO)O)O)O |
| InChI | 1S/C17H20N4O6/c1-7-3-9-10(4-8(7)2)21(5-11(23)14(25)12(24)6-22)15-13(18-9)16(26)20-17(27)19-15/h3-4,11-12,14,22-25H,5-6H2,1-2H3,(H,20,26,27)/t11-,12+,14-/m0/s1 AUNGANRZJHBGPY-SCRDCRAPSA-N |
| Кодекс Алиментариус | E101 |
| ChEBI | 17015 |
| ChemSpider | 431981 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
| Медиафайлы на Викискладе | |
Рибофлави́н (лактофлавин, витамин B2) — один из наиболее важных водорастворимых витаминов, кофермент многих биохимических процессов. Используется в качестве пищевого красителя, входит в Кодекс Алиментариус под кодом E101.
Физические свойства[править | править код]
Рибофлавин представляет собой игольчатые кристаллы жёлто-оранжевого цвета, собранные в друзы, горького вкуса. Рибофлавин является производным гетероциклического соединения изоаллоксазина, связанного с многоатомным спиртом рибитом.
Хорошо[1]растворим в воде, устойчив в кислых растворах, но легко разрушается в нейтральных и щелочных. Чувствителен к видимому и УФ-излучению и сравнительно легко подвергается обратимому восстановлению.
Химические свойства[править | править код]
Рибофлавин является биологически активным веществом, играющим важную роль в поддержании здоровья человека. Биологическая роль рибофлавина определяется вхождением его производных флавинмононуклеотида (ФМН) и флавинадениндинуклеотида (ФАД) в состав большого числа важнейших окислительно-восстановительных ферментов в качестве коферментов.
Флавиновые ферменты принимают участие в окислении жирных, янтарной и других кислот; инактивируют и окисляют высокотоксичные альдегиды, расщепляют в организме чужеродные D-изомеры аминокислот, образующиеся в результате жизнедеятельности бактерий; участвуют в синтезе коферментных форм витамина B6 и фолацина; поддерживают в восстановленном состоянии глутатион и гемоглобин.
В ферментах коферменты функционируют как промежуточные переносчики электронов и протонов, отщепляемых от окисляемого субстрата.
Недостаток рибофлавина в организме человека[править | править код]
Витамин B2 необходим для образования эритроцитов, антител, для регуляции роста и репродуктивных функций в организме. Он также необходим для здоровья кожи, ногтей, роста волос и в целом для здоровья всего организма, включая функцию щитовидной железы.
Внешними проявлениями недостаточности рибофлавина у человека являются поражения слизистой оболочки губ с вертикальными трещинами и слущиванием эпителия (хейлоз), изъязвления в углах рта (ангулярный стоматит), отёк и покраснение языка (глоссит), себорейный дерматит на носогубной складке, крыльях носа, ушах, веках. Часто развиваются также изменения со стороны органов зрения: светобоязнь, васкуляризация роговой оболочки, конъюнктивит, кератит и в некоторых случаях — катаракта. В ряде случаев при авитаминозе имеют место анемия и нервные расстройства, проявляющиеся в мышечной слабости, жгучих болях в ногах и др.
Основные причины недостатка рибофлавина у человека — недостаточное потребление пищи, содержащей этот витамин; неправильное хранение и приготовление пищи, содержащей данный витамин, вследствие чего содержание витамина резко уменьшается; хронические заболевания желудочно-кишечного тракта, приём медикаментов, являющихся антагонистами рибофлавина.
| Продукт питания | Содержание рибофлавина, мг/100 г продукта: |
|---|---|
| печень и почки | 2,80—4,66 |
| дрожжи | 2,07—4,0 |
| яйца | 0,30—0,80 |
| миндаль | 0,80 |
| шампиньоны | 0,4 |
| белые грибы | 0,3 |
| лисички | 0,3 |
| творог | 0,30—0,50 |
| брокколи | 0,3 |
| белокочанная капуста | 0,25 |
| гречневая крупа | 0,24 |
| молоко | 0,13—0,18 |
| мясо | 0,15—0,17 |
| очищенный рис, макаронные изделия, белый хлеб, большинство фруктов и овощей | 0,03—0,05 |
Человеческий организм не накапливает рибофлавин, и любой избыток выводится вместе с мочой. При избытке рибофлавина моча окрашивается в ярко-жёлтый цвет.
Нормы потребления рибофлавина[править | править код]
| Пол | Возраст | Суточная норма рибофлавина (витамина B2)[2] |
|---|---|---|
| Младенцы | до 6 месяцев | 0,4 мг/день |
| Младенцы | 7 — 12 месяцев | 0,6 мг/день |
| Дети | 1 — 3 года | 0,9 мг/день |
| Дети | 4 — 8 лет | 1,3 мг/день |
| Дети | 9 — 13 лет | 1,9 (мальчики) 1,7 (девочки) мг/день |
| Мужчины | 14 лет и старше | 1,7 мг/день |
| Женщины | 14 лет и старше | 1,8 мг/день |
| Женщины | беременные кормящие | 2,0 мг/день 2,2 мг/день |
В пожилом возрасте и при усиленных физических нагрузках потребность возрастает.
Получение в промышленности[править | править код]
В промышленности рибофлавин получают химическим синтезом из 3,4-диметиланилина и рибозы или микробиологически, например, с использованием гриба Eremothecium ashbyi или используя генетически изменённые бактерии Bacillus subtilis.
Фармакологическое применение[править | править код]
Препараты рибофлавин и ФМН применяют для профилактики и лечения недостаточности витамина B2, при кожных заболеваниях, вяло заживающих ранах, заболеваниях глаз, нарушении функции желудочно-кишечного тракта, диабете, анемиях, циррозе печени.
Применение в пищевой промышленности[править | править код]
В пищевой промышленности рибофлавин используется для обогащения некоторых продуктов питания витамином B2 или как пищевой краситель (E101).
Рибофлавин зарегистрирован в качестве пищевой добавки Е101.
Синонимы[править | править код]
Лактофлавин, овофлавин, гепатофлавин, вердофлавин, урофлавин, бефлавин, бефлавит, бетавитам, флаваксин, флавитол, лактобен, рибовин, витафлавин, витаплекс В2. Большинство из этих названий указывают на источник, из которого данный витамин был исходно выделен, то есть молоко, яйца, печень, растения, моча.
Формы выпуска[править | править код]
Порошок; таблетки по 0,002 г в профилактических целях; таблетки по 0,005 и 0,01 г в лечебных целях. Ампулы 1 мл — раствор для внутримышечного введения.
Литература[править | править код]
- Н. С. Зефиров, Н. Н. Кулов и др. Химическая энциклопедия. Том 4. — Москва: Научное издательство «Большая российская энциклопедия», 1995. — С. 266—267. — ISBN 5-85270-092-4
Примечания[править | править код]
- ↑ Т. Т. Березов. Биологическая химия / Под редакцией академика АМН СССР С. С. Дебова. — 2е, переработанное и дополненное.
- ↑ Riboflavin.
Источник
[06-313]
Витамин B2 (ФАД)
1350 руб.
Определение концентрации флавинадениндинуклеотида (ФАД), являющегося коферментом витамина В2, в образце венозной крови для изучения и оценки обменных процессов и реакций, протекающих с участием этого витамина, и выявления возможных нарушений в них.
Синонимы русские
Рибофлавин, лактофлавин, флавинадениндинуклеотид (ФАД).
Синонимы английские
Riboflavin, Vitamin B2, Lactoflavin, flavin adenine dinucleotide (FAD).
Метод исследования
Высокоэффективная жидкостная хроматография с тандемным масс-спектрометрическим детектированием (ВЭЖХ-МС/МС)
Единицы измерения
Нмоль/л (наномоль на литр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Детям в возрасте до 1 года не принимать пищу в течение 30-40 минут до исследования.
- Не принимать пищу в течение 2-3 часов до исследования, можно пить чистую негазированную воду.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Витамин В2, или рибофлавин, — один из важнейших участников множества биохимических процессов в организме. Он необходим для жизнедеятельности клеток и тканевого дыхания, обменных и окислительно-восстановительных реакций.
Флавинадениндинуклеотид (ФАД), наряду с флавинмононуклеотидом, — важнейшее производное рибофлавина, определяет его биологическую роль. ФАД является коферментом, то есть активным центром, играющим непосредственную роль в протекании тех или иных реакций. Входит в состав ферментов, участвующих в окислении жирных кислот, цикле Кребса, транспорте необходимых веществ для энергетических процессов в мозге и скелетных мышцах и т. д. Все эти процессы происходят на клеточном уровне, от таких реакций зависит нормальное функционирование каждого органа и всего организма в целом.
Суточная потребность рибофлавина меняется в зависимости от возраста. В среднем для взрослого человека она составляет около 1,7-1,8 мг в день и несколько выше в период полового созревания, беременности, при усиленных физических нагрузках и в пожилом возрасте. Витамин В2 содержится в продуктах растительного (ячмень, овощи, какао) и животного происхождения (молоко, яйца, печень, почки).
Рибофлавин играет важнейшую роль в образовании эритроцитов, компонентов иммунной системы, гормональном контроле роста и половой функции. Также необходим для нормального состояния кожи, ногтей и волос.
При недостаточности рибофлавина повышается риск развития анемии, неврологических нарушений, ухудшения состояния волос, ногтей, кожи, воспалительных и дегенеративно-дистрофических заболеваний глаз. Клинические проявления дефицита витамина В2: дерматит, хейлит (поражение слизистой губ), ангулярный стоматит (трещины в углах рта), глоссит (болезненный язык), конъюнктивит, кератит и в некоторых случаях катаракта. Неврологические нарушения могут быть представлены мышечным напряжением, болями в ногах.
Определение концентрации флавинадениндинуклеотида витамина В2 проводится методом жидкостной хроматографии с тандемным масс-спектрометрическим детектированием. Суть его заключается в выделении нужного вещества на основании физико-химических свойств из образца венозной крови, его ионизации и сортировке полученных ионов в зависимости от массы с последующим их анализом. Метод является одним из самых современных, обладает высокой чувствительностью, позволяет анализировать большое количество веществ без ограничения по их физико-химическим свойствам за относительно небольшой промежуток времени.
Для чего используется исследование?
- Для диагностики недостаточности, дефицита или возможности передозировки витамина B2 в организме.
- Для контроля эффективности заместительной терапии препаратами витаминов группы В.
Когда назначается исследование?
- При клинических проявлениях недостаточности рибофлавина: покраснении и трещинах в углах рта, себорейном дерматите, болезненном красном языке, ухудшении состояния волос и ногтей, развитии воспалительных заболеваний глаз неясной этиологии, некоторых неврологических нарушениях.
- При хронических заболеваниях желудочно-кишечного тракта и нарушении всасывания поступающих с пищей веществ.
- При длительном приеме лекарственных препаратов, снижающих уровень витамина В2 (например, антидепрессантов, барбитуратов и др.).
Что означают результаты?
Референсные значения
— В цельной крови 116,0 — 393,0 нмоль/л
— В плазме 56,0 — 97,00 нмоль/л
Причины повышения уровня витамина В2 (ФАД):
- применение заместительной терапии препаратами рибофлавина – как парентерально, так и внутрь.
Причины понижения уровня витамина В2 (ФАД):
- недостаточное употребление продуктов, содержащих рибофлавин;
- хронические заболевания желудочно-кишечного тракта с нарушением всасывания поступающих с пищей веществ.
Что может влиять на результат?
- Уровень витамина В2 (ФАД) может снижаться при употреблении алкоголя и некоторых лекарственных препаратов (барбитураты, антидепрессанты, тиреоидные гормоны и др.).
- Антихолинергические препараты могут увеличивать всасывание рибофлавина из кишечника в кровь.
Важные замечания
- Дефицит витамина B2 нередко сочетается с дефицитом других водорастворимых витаминов и редко встречается изолированно.
- Определение уровня витамина B2 в форме ФАД в плазме крови рассматривается как вспомогательный лабораторный маркер для оценки достаточности уровня витамина B2. В качестве базового маркера для оценки уровня витамина B2 рекомендовано определение витамина B2 в форме ФАД в цельной крови.
Также рекомендуется
- Клинический анализ крови: общий анализ, лейкоцитарная формула, СОЭ (с микроскопией мазка крови при выявлении патологических изменений)
- Витамин В1 (тиамин-пирофосфат)
- Витамин В2 (рибофлавин)
- Витамин B3 (ниацин, никотинамид)
- Витамин В5 (пантотеновая кислота)
- Витамин В6 (пиридоксаль-5-фосфат)
- Витамин В12 (цианокобаламин)
- Витамин С (аскорбиновая кислота)
Кто назначает исследование?
Терапевт, невролог, офтальмолог, дерматовенеролог, гастроэнтеролог, врач общей практики, эндокринолог.
Литература
- Pinto JT, Zempleni J. Riboflavin. Adv Nutr. 2016 Sep 15;7(5):973-5.
- Powers HJ, Corfe BM, Nakano E. Riboflavin in development and cell fate. Subcell Biochem. 2012;56:229-45.
- Kuppuraj G, Kruise D, Yura K. Conformational behavior of flavin adenine dinucleotide: conserved stereochemistry in bound and free states. J Phys Chem B. 2014 Nov 26;118(47):13486-97.
- Robbins JM, Souffrant MG, Hamelberg D, Gadda G, Bommarius AS. Enzyme-Mediated Conversion of Flavin Adenine Dinucleotide(FAD) to 8-Formyl FAD in Formate Oxidase Results in a Modified Cofactor with Enhanced Catalytic Properties. Biochemistry. 2017 Jul 25;56(29):3800-3807.
Источник
